LIMS vs LIS : lequel correspond vraiment à votre laboratoire ?
le 16 Juin de 14h à 15h

Il existe une confusion fréquente entre les notions de LIMS (Laboratory Information Management System) et LIS (Laboratory Information System) ou SIL (Système d’information de laboratoire) en français, et une tendance à les utiliser comme des synonymes. Pourtant, ces deux systèmes répondent à des besoins fondamentalement différents.
Le LIS est principalement utilisé dans les laboratoires médicaux et hospitaliers, où il organise le suivi des patients, la gestion des prescriptions et la diffusion fiable des résultats cliniques. Le LIMS, en revanche, trouve sa place dans de nombreux secteurs (industrie, production pharmaceutique, agroalimentaire, chimique, environnemental, etc.). Sa mission est de gérer le cycle de vie des échantillons, d’assurer la traçabilité des analyses et d’optimiser les processus, en mettant l’accent sur la performance opérationnelle plutôt que sur le patient.
Voici un décryptage clair et opérationnel pour comprendre ce qui les distingue, et comment orienter son choix avec discernement.
LIMS vs LIS : deux logiciels, deux philosophies
Le LIS : centré sur le patient et le diagnostic
Le LIS s’est développé historiquement dans le secteur médical. Sa finalité première est de gérer les analyses biologiques liées aux patients, en mettant l'accent sur la sécurité des informations personnelles identifiables.
Les laboratoires hospitaliers faisant face à une augmentation rapide du volume d’analyses, il devient alors indispensable d’enregistrer les résultats de façon électronique, de les centraliser et de les transmettre rapidement aux services cliniques. Le LIS naît donc d’un besoin opérationnel très concret : fiabiliser la saisie, éviter les erreurs de retranscription et accélérer l’acheminement des comptes rendus.
Sa logique est clinique :
- Gestion des dossiers patients
- Suivi des prescriptions
- Validation et diffusion des résultats
- Conformité aux normes médicales et réglementaires
- Intégration avec les systèmes hospitaliers (HIS, DPI, etc.)
Le LIS structure donc le parcours de l’échantillon dans une perspective de diagnostic.
Aujourd’hui, le périmètre s’est élargi. Au-delà de l’enregistrement et de la diffusion des résultats, les LIS intègrent des fonctionnalités de gestion.
Le LIMS : orienté échantillon, processus et qualité
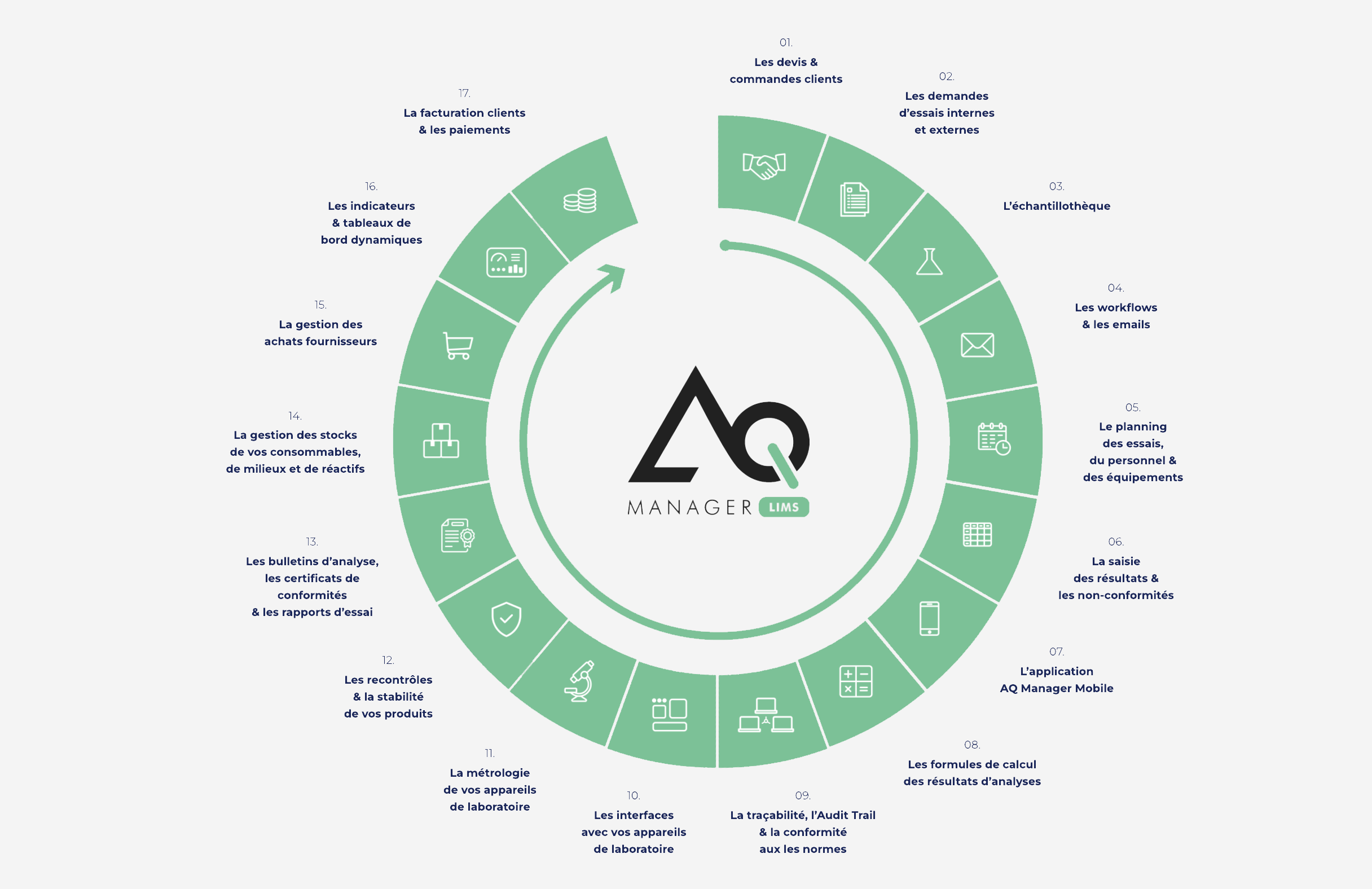
Le LIMS, lui, est né dans des environnements industriels, pharmaceutiques, agroalimentaires ou environnementaux. Sa mission est plus large : gérer le cycle de vie des échantillons, piloter les flux analytiques, assurer la traçabilité et optimiser les processus.
Il s’est développé plus tard, à mesure que les exigences réglementaires et les besoins en reporting se sont intensifiés. Les environnements soumis aux référentiels qualité (ISO, GxP, BPL, etc.) exigeaient une documentation plus dense, des procédures plus complexes, une traçabilité fine et exploitable.
Il répond à cette réalité : workflows configurables, gestion documentaire associée aux méthodes, audit trail détaillé, consolidation des données analytiques pour le reporting et les indicateurs de performance.
Sa logique est opérationnelle et industrielle :
- Enregistrement et suivi des échantillons
- Gestion des méthodes analytiques
- Planification des tests
- Contrôle qualité
- Gestion documentaire
- Conformité réglementaire (ISO, GLP, GMP…)
- Intégration avec ERP, MES ou systèmes qualité
Le LIMS est un outil de maîtrise industrielle. Il vise la performance, la traçabilité, la robustesse des processus.
Les fonctionnalités : convergences et divergences
Fonctionnalités communes au LIS et au LIMS
Il serait faux d’opposer radicalement LIMS et LIS. Ils partagent un socle fonctionnel :
- Gestion des échantillons
- Traçabilité des analyses
- Validation des résultats
- Génération de rapports
- Contrôle des accès
- Conformité réglementaire
- Archivage sécurisé des données
Dans les deux cas, la fiabilité et l’intégrité des données sont non négociables.
Fonctionnalités spécifiques au LIS
Le LIS intègre des fonctionnalités spécifiques au monde médical :
- Gestion des identités patients
- Compatibilité avec les standards de santé (HL7, etc.)
- Interprétation biologique et commentaires médicaux
- Transmission sécurisée aux médecins et hôpitaux
- Gestion des urgences et priorités cliniques
- Facturation et nomenclature des actes
Le résultat est un élément de diagnostic. Le système doit donc intégrer une dimension clinique et médico-légale forte.
Chaque information – antécédents médicaux, résultats d'examens, ordonnances, etc. – doit être correctement associée au patient concerné. Le système garantit la sécurité du stockage des données sensibles et leur accessibilité pour la prise de décision clinique, tout en assurant la conformité aux réglementations en matière de santé.
Fonctionnalités spécifiques au LIMS
Le LIMS, de son côté, offre une profondeur fonctionnelle orientée production et qualité :
- Gestion multi-sites, multilingue, et multi-laboratoires
- Automatisation des flux analytiques
- Planification des campagnes de tests et d’analyse
- Gestion des stocks
- Gestion des équipements et métrologie
- Suivi des non-conformités
- Audit trail avancé
- Intégration avec ERP, CRM ou systèmes industriels
Il est conçu pour absorber des volumes importants, gérer des processus complexes et soutenir des démarches qualité exigeantes.
Associé à un ELN (Electronic Laboratory Notebook/Cahier électronique de laboratoire), il va plus loin encore : structuration des protocoles, traçabilité des essais en R&D, historisation des versions de méthodes, capitalisation du savoir expérimental. Le LIMS sécurise et industrialise la donnée ; l’ELN capture et formalise l’intelligence scientifique. Ensemble, ils couvrent à la fois l’exécution analytique et la conception expérimentale.
Les enjeux réglementaires : deux univers normatifs
Un LIS opère dans un cadre fortement médicalisé :
- Accréditations spécifiques aux laboratoires de biologie
- Obligations de confidentialité liées aux données de santé
- Exigences nationales de traçabilité clinique
La dimension juridique y est particulièrement sensible.
Le LIMS, lui, s’inscrit dans des environnements réglementaires industriels exigeants également :
- ISO 17025, ISO 9001, etc.
- BPF/GMP
- GLP
- Réglementations environnementale, pharmaceutiques, chimiques, etc.
La conformité y est également critique, mais elle s’articule autour de la qualité produit et des processus.

Les profils d’utilisateurs
Un LIS est principalement utilisé par :
- Biologistes médicaux
- Techniciens de laboratoire hospitalier
- Secrétaires médicales
- Médecins prescripteurs
- Etc.
Un LIMS s’adresse davantage à :
- Responsables qualité
- Responsables et techniciens de labo
- Ingénieurs R&D
- Responsables de production
- Responsables réglementaires
- Responsables des achats
Cette différence d’audience influence fortement l’ergonomie et les priorités fonctionnelles.
LIMS : ergonomie, formation des utilisateurs et intégration au système d’information
Une interface accessible pour tous les profils du laboratoire
Dans un laboratoire, les profils utilisateurs sont variés : techniciens, responsables qualité, ingénieurs R&D, responsables de production, équipes qualité, etc.. Tous n’utilisent pas les outils informatiques de la même manière et n’ont pas les mêmes besoins au quotidien.
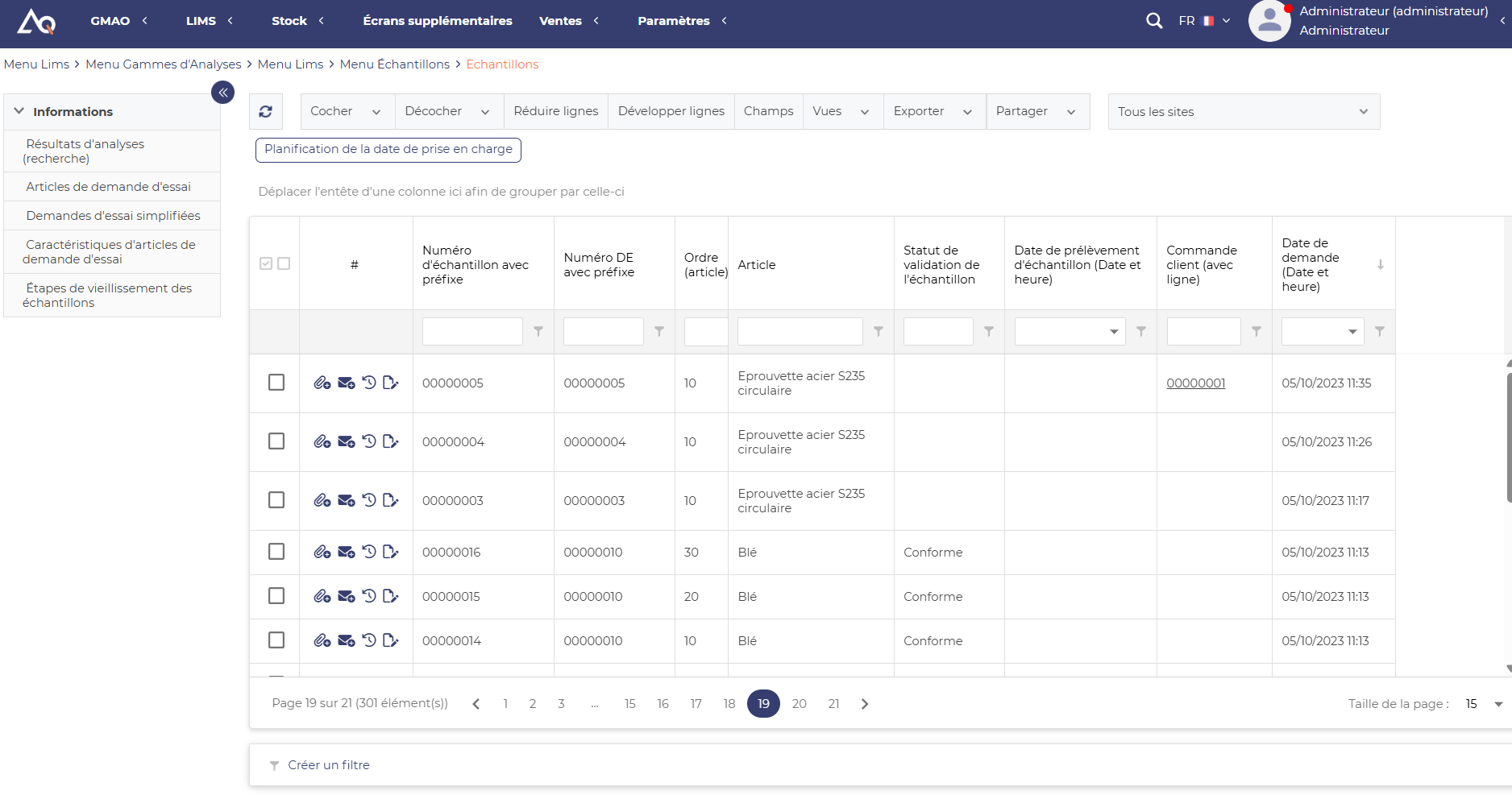
Le LIMS propose généralement des interfaces personnalisables et des menus graphiques et intuitifs. Les écrans sont organisés autour des tâches courantes : enregistrement des échantillons, suivi des analyses, validation des résultats ou consultation d’indicateurs.
Cette organisation facilite la prise en main et permet aux utilisateurs de retrouver rapidement les informations dont ils ont besoin.
Une interface bien conçue contribue aussi à limiter les erreurs de saisie et à rendre les workflows plus fluides pour les équipes du laboratoire.
Formation et accompagnement des équipes
La mise en place d’un LIMS implique souvent une évolution des habitudes de travail. Les équipes doivent se familiariser avec de nouveaux processus et comprendre la logique du système.
Pour cette raison, les projets LIMS incluent généralement des phases de formation adaptées aux différents profils du laboratoire. Les sessions de formation permettent à chacun de comprendre comment utiliser l’outil dans son périmètre.
Un accompagnement lors du déploiement facilite aussi l’appropriation du système. Les équipes peuvent poser leurs questions, ajuster certains paramètres et intégrer progressivement le LIMS dans leurs pratiques quotidiennes.
Un système connecté à l’écosystème de l’entreprise
Dans de nombreux environnements industriels, le LIMS fonctionne en lien avec d’autres outils du système d’information. Les échanges de données permettent de fluidifier les processus et d’éviter les ressaisies.
Le LIMS peut par exemple s’intégrer avec :
- ERP pour la gestion des ressources et de la production
- MES pour le suivi des opérations industrielles
- Systèmes qualité ou de gestion documentaire
- Instruments analytiques du laboratoire
Ces connexions permettent de centraliser les données analytiques et de les rendre accessibles aux différentes équipes.
Comment choisir entre LIMS et LIS : les bonnes questions à se poser
Avant de trancher entre LIMS et LIS, il faut clarifier plusieurs points :
- Votre activité est-elle centrée sur des patients ou sur des produits ?
- Quelles sont vos obligations réglementaires principales ?
- Travaillez-vous en environnement hospitalier ou industriel ?
- Avez-vous besoin d’intégrations avec des systèmes médicaux ou industriels ?
- Quels sont vos objectifs prioritaires : diagnostic rapide, optimisation de la production, conformité qualité, traçabilité multi-sites, etc. ?
Un choix pertinent repose sur une analyse fonctionnelle détaillée.
| Question | LIS | LIMS |
| Que suivez-vous principalement ? | Données liées aux patients, données cliniques, résultats d'examens médicaux, diagnostics, etc. | Données liées aux échantillons et lots : matières premières, produits en cours, résultats de contrôle qualité, données issues de la recherche, etc. |
| Quel est votre principal cadre de conformité ? | Normes et régulations du secteur médical : HIPAA, CLIA, CAP, confidentialité de données de santé. | Réglementations industrielles et qualité : FDA, GLP, BLP, BPF, ISO, exigences qualité spécifiques aux industries pharmaceutiques, agroalimentaires, chimiques, cosmétiques, etc. |
| Avec quels autres systèmes devez-vous vous connecter ? | Systèmes hospitaliers et administratifs : dossiers médicaux électroniques (EHR), systèmes d’information hospitaliers, gestion des assurances et facturation. | Systèmes industriels et analytiques : instruments de laboratoire, ERP (gestion des ressources d’entreprise), MES (systèmes de gestion de production), laboratoires partenaires ou clients. |
| Quels types de rapports ou résultats sont nécessaires ? | Rapports cliniques : résultats des patients, synthèses diagnostiques permettant la prise de décision médicale rapide et fiable. | Documents qualité et conformité : certificats d’analyse (COA), rapports de contrôle qualité, documentation réglementaire nécessaire à la conformité des processus. |
| Qui utilise le système au quotidien ? | Professionnels de santé : médecins, infirmiers, pathologistes, techniciens médicaux qui ont besoin d’informations cliniques fiables et à jour. | Équipes opérationnelles : analystes de laboratoire, responsables qualité (QA), personnels de production, chercheurs en R&D, responsables conformité. |
Conclusion : choisir avec lucidité
Le débat LIMS ou LIS, au fond, ce n’est finalement pas qu’une bataille d’acronymes mais surtout une question de réalité opérationnelle sur le terrain.
Ce qui compte, c’est de trouver un logiciel qui colle à votre manière de travailler, à vos flux, à vos contraintes, à la pression réglementaire que vous avez réellement sur les épaules. Un outil peut être excellent… et complètement inadapté à votre réalité.
LIMS et LIS répondent tous deux à des logiques différentes, et surtout à des environnements différents. Confondre les deux, c’est prendre le risque de faire un choix bancal et les ajustements tardifs coûtent toujours plus cher !
Découvrez plus d’articles
-
 LIMS Actualités / Nouveautés
LIMS Actualités / NouveautésLIMS open source : une idée séduisante, mais à quel prix ?
Mathilde Lebrun -
 GMAO Actualités / Nouveautés
GMAO Actualités / NouveautésCombien coûte réellement un logiciel de GMAO ?
Mathilde Lebrun -
 LIMS Actualités / Nouveautés
LIMS Actualités / NouveautésComment optimiser vos coûts d’analyse sans compromettre la qualité ?
Mathilde Lebrun



